1. 서 론
2. 실 험
2.1 태양광 폐모듈로부터 실리콘 회수
2.2 재활용실리콘을 이용한 질화규소 합성
3. 결과 및 토의
3.1 회수 실리콘의 물리ㆍ화학적 특성
3.2 질화 반응 거동 및 Si3N4 합성결과
3.3 질화 반응 메커니즘 고찰
4. 결 론
1. 서 론
태양광 발전은 탄소중립 실현을 위한 핵심 수단으로 주목받으며, 전 세계적으로 보급이 빠르게 확산되고 있다. 2025년 IEA 보고서(Global Energy Review 2025)에 따르면, 2024년 한 해 동안 태양광 발전(PV) 신규 설치 용량은 전년 대비 약 30% 증가하여 총 약 550 GW에 달하였다. 이러한 성장을 바탕으로, 전 세계 누적 태양광 설치 용량은 약 2.2 TW에 도달한 것으로 추정된다1). 이와 같은 급속한 보급 확산은 향후 태양광 폐모듈의 대량 발생을 불러올 것으로 예측되며, 부적절한 처리 시 매립에 따른 토양·지하수 오염, 소각에 따른 온실가스 및 유해물질 배출 등 환경에 심각한 악영향을 미칠 우려가 있다. 이에 따라, 우리나라 및 유럽연합(EU)을 포함한 많은 국가들은 태양광 모듈에 대한 생산자책임재활용제도(Extended Producer Responsibility, EPR)를 의무화함으로써, 폐모듈의 회수·재활용 체계를 제도적으로 뒷받침하고 있다2).
태양광 폐모듈내의 태양전지는 일반적으로 유리 기판, EVA, 결정질 실리콘(c-Si) 태양전지 셀, EVA, 백시트로 구성되어 있다. 이중 결정질 실리콘은 태양전지의 핵심 광 흡수층으로서 전체 모듈무게의 약 3 ~ 5%를 차지한다. 폐모듈에서 실리콘을 회수하여 재사용하는 것은 자연 상태에서 광석을 채굴 제련하여 채굴·제련하여 고순도화하는 과정에 비해 에너지 소비와 온실가스 배출을 크게 줄일 수 있으며, 경제적 가치 또한 높다. Lee et al. (2025)3)의 연구에 따르면 1톤의 폐태양광 모듈에는 약 137 kg의 알루미늄, 30 kg의 고순도 실리콘, 7 kg의 구리, 300 g의 은이 포함되어 있어 동일한 무게의 구리광석 대비 2배 이상의 경제적 가치를 지니며, Riahi et al. (2023)4)의 연구에서는 태양광 폐모듈에서 회수한 실리콘을 정제·용융하는 경우 공정 내에서 배출되는 CO2의 양은 1.15 kg CO2e/kg-Si로, 기존 실리콘 생산(4.7–5.0 kg CO2e/kg-Si)에 비해 약 75% 감소한다고 보고한다. 따라서 태양광 폐모듈에서 실리콘을 회수하여 다른 고부가가치 산업의 원료로 활용한다면, 환경적ㆍ경제적인 측면에서 모두 긍적적인 효과를 기대할 수 있다.
태양광 폐모듈에서 회수한 재활용 실리콘(r-Si)은 이차전지 음극재5), 태양광용 폴리실리콘6), SiC7) 및 질화규소(Si3N4)8)와 같은 세라믹 소재 등 다양한 분야로 활용이 가능하다. 이중 태양광용 잉곳 및 웨이퍼는 6 N 이상의 초고순도가 요구되는 반면, 세라믹 합성의 경우 3 N 이상의 순도 확보만으로도 실용적인 활용이 가능하다9). 특히 Si3N4는 우수한 기계적 강도, 내열성, 내마모성을 갖추고 있어 절삭공구, 베어링 등에 널리 활용되고 있으며10), 최근에는 우수한 열전도도를 바탕으로 전기차의 파워 모듈 및 인버터용 방열기판 소재로도 주목받고 있다11). 그러나 Si3N4원료는 국내생산 기반이 미약하여, 현재 대부분을 일본, 중국 등 해외수입에 의존하고 있기에 자원 순환형 소재의 개발과 국산화 연구의 필요성은 증가하고 있다. 따라서 r-Si을 원료로 활용하여 Si3N4를 합성한다면, 자원 순환과 수입의존도 저감 측면에서 큰 의의가 있을 것으로 기대된다. 그러나 아직까지 r-Si을 이용해 Si3N4를 합성한 연구 사례는 보고된 바 없어 검증이 필요한 상황이다.
Si3N4를 합성하는 방법에는 탄소열 환원질화법12), 디이미드열분해법13) 등이 있으나, 본 연구에서는 폐태양광 모듈에서 회수한 r-Si를 원료로 하여 질소 분위기에서 직접 반응시키는 ‘직접 질화(direct nitridation)’ 방식을 택하였다. 탄소열 환원질화법은 SiO2와 탄소를 혼합하여 고온에서 환원·질화시키는 방식으로, 환원제(탄소) 투입에 따른 불순물(C, O 잔존)의 문제가 있으며 장시간의 고온 공정이 요구된다. 디이미드 열분해법은 Si(NH)2와 같은 디이미드 전구체를 합성한 후, 이를 열분해하여 Si3N4를 얻는 방식으로, 고순도 분말을 얻을 수 있으나 전구체 합성 과정이 복잡하고 비용이 높다는 단점이 있다. 반면, 직접 질화법은 별도의 환원제나 전구체 합성을 거치지 않고 실리콘 원료 자체를 질소와 직접 반응시켜 Si3N4를 얻는 단순하고 효율적인 방법이라는 장점이 있다. 일반적인 직접 질화 공정은 반응 속도가 느려 장시간 반응 시간이 요구된다는 장애요소가 있으나14), 본 연구에서는 실리콘 융점(1414℃) 이상의 고온 영역에서 질화 반응을 유도하여 반응 속도를 향상시키고, 보다 효율적으로 Si3N4를 합성하고자 하였다. 이를 통해 r-Si의 세라믹 원료화 가능성을 검증하고, 자원 순환 및 소재 자립 측면에서의 활용 가능성을 제시하고자 한다.
2. 실 험
2.1 태양광 폐모듈로부터 실리콘 회수
본 연구에서는 2000년대 상용화된 태양광 폐모듈을 사용하였다. 사용된 모듈은 Suntech사의 STP200-18/Ub 모델로, 크기는 1,482 × 992 mm2이며 태양전지는 6 × 9 배열의 총 54셀로 구성되어 있다. 해당모듈은 다결정 실리콘 기반의 Al-BSF 구조로 제작되었으며, 현재 수명이 종료되어 폐모듈로 배출되고 있는 대표적인 세대의 모듈에 해당한다15). 모듈은 외부에 알루미늄 프레임과 정션박스를 포함하고 있으며, 내부는 Glass / EVA / cell / EVA / backsheet 구조로 적층되어 있다. 알루미늄 프레임과 정션박스는 수작업으로 분리하였고, 핫나이프 방식의 스크레이퍼를 이용하여 유리와 나머지 적층 시트를 분리하였다16). 분리된 적층시트는 단일 cell 크기(약 156 × 156 mm2)로 제단하여 로터리커터밀(CTHC-0707, CRUTEC/Republic of Korea) 장비를 이용하여 파쇄를 진행하였다. 파쇄는 400 rpm의 속도로 수행되었으며, cell은 10초 간격으로 한 장씩 투입하였다. 총 54개의 cell을 모두 투입한 뒤, 추가로 600초간 파쇄를 진행하였다. 분쇄된 실리콘 입자는 체가름기 장비를 사용한 Sieving공정을 실시하였다. 체눈 크기 0.5 mm의 체를 이용한 Sieving을 2 mm 진폭으로 5분간 진행하였으며, 해당 과정에서 연성을 가지는 구리리본은 큰 조각으로 확보되어, 일차적으로 분리된다. 이후 600℃ 1시간동안 연소과정을 진행하여 유기물이 제거된 r-Si을 확보하였다17). 회수된 r-Si에는 다양한 금속 불순물이 포함되어 있으며, 이는 고순도 실리콘 확보에 직접적인 장애 요인으로 작용하여 최종 순도에 악영향을 미친다. 이러한 불순물을 제거하기 위해 2-step 습식 에칭 공정을 적용하였다. 첫 번째 단계에서는 HCl 용액을 사용하여 주 타겟 불순물인 Al을 포함한 금속 불순물을 제거하였으며, 두 번째 단계에서는 HNO3 용액 처리를 통해 Ag 및 잔여 금속 성분을 추가로 제거하였다. 구체적으로, 분말 10 g을 기준으로 HCl 에칭은 36 wt% 용액 1 L에서 20분간 수행하였으며, HNO3 에칭은 동일 농도의 용액 1 L에서 30분간 수행하였다18).
2.2 재활용실리콘을 이용한 질화규소 합성
회수된 r-Si 분말은 Si3N4 합성에 적합하도록 입도를 확보하기 위해 볼 밀링 공정을 거쳤다. 볼 밀링은 지르코니아(ZrO2) 용기와 볼을 사용하였으며, 직경 10 mm와 3 mm의 볼을 1:1로 혼합하여 적용하였다. 볼과 분말의 무게비(BPR, ball-to-powder ratio)는 10:1로 설정하였고, 에탄올을 이용한 습식 조건에서 200 rpm으로 20시간 동안 진행하였다. 볼 밀링 전후의 입도 분포는 레이저 회절식 입도분석기(PSA, Mastersizer 2000, Malvern/UK)를 이용하여 측정하였으며, 형상 및 미세구조 변화는 주사전자현미경(FE-SEM, S-4800, Hitachi/Japan)을 통해 비교·분석하였다. 에칭 및 볼밀링 공정 후 회수된 r-Si의 순도는 유도결합플라즈마 분광분석기(ICP-OES, iCAP 6000 Duo, Thermo Fisher Scientific/USA)를 이용하여 확인하였다. 적절한 입도 분포가 확보된 r-Si 분말은 튜브형 전기로를 이용하여 질화규소 합성에 사용하였다. 사용된 전기로는 내경 60 mm, 길이 1000 mm의 튜브를 사용하여 반응을 진행하였으며, 이에 따른 로용적은 약 2.83 L이었다. 반응 분위기는 95.10124 v% N2와 4.89876 v% H2로 구성된 5N급 이상의 혼합가스를 공급하여 형성하였다. 이 혼합가스는 공급업체로부터 산소 및 수분함량이 각각 1 ppm 미만으로 보증됨을 확인하였다. 이때, 소량의 H2는 환원분위기를 조성하여 r-Si 표면에 존재하는 산화막(SiO2)을 제거하고, 질소와 반응성을 향상시키는 역할을 한다19). 열처리 전 분말을 전기로에 투입한 후 챔버 내 불순물을 제거하기 위해 진공 및 퍼지 공정을 수행하였다. 진공펌프를 이용하여 5 × 10-4 Torr까지 진공 배기를 진행하여 내부 기체 불순물을 최소화한 후 혼합가스를 1 atm 수준까지 주입한 후 다시 배출하는 진공-가스 충진 공정을 2회 반복하였으며 해당과정은 약 20분 소요되었다. 이후 out line valve를 개방하여 자연스러운 혼합가스의 흐름을 만들었으며, 질화공정은 1 atm 하에서 진행하였다. 이때, 혼합가스의 유량은 800 sccm으로 유지하였다. 합성 공정은 약 1 g의 r-Si 분말을 알루미나 보트에 담아 Table 1에 제시된 조건에 따라 질화 처리를 각각 수행하였다. 승온 속도는 10℃/min으로 설정하였다. 이후 질화 공정은 1350℃에서의 표면 질화 단계와 1450℃에서의 고온 질화 단계의 2단계(2-step) 열처리 공정으로 구성되었으며, 각각 Table 1의 조건에 맞추어 진행하였다. 열처리가 끝난 후 모든 시료는 전기로 내에서 자연 냉각시켰다. 특히 1450℃ 승온조건에서는 반드시 1350℃에서 1 h 전처리를 수행하였다. 이는 내부 실리콘이 용융되기 전 단계에서 입자표면에 Si3N4 피막을 우선 형성함으로써, 이후 1450℃에서 Si가 용융될 때 분말의 구조적 지지체로 작용하도록 유도하기 위함이다. 이러한 전처리 과정은 과도한 응집을 억제하고, 질소의 균일한 확산을 가능하게 한다20).
Table 1.
Nitridation conditions for each sample
질화실험이 완료된 시료는 X선 회절분석(XRD, MiniFlex 600, Rigaku/Japan)을 수행하였고, Rigaku사의 SmartLab Studio II 소프트웨어를 이용하여 존재하는 상의 피크면적을 산출하였다21). 이를 기반으로 Jovanovic et al. (1994)이 제시한 방법을 적용하여 각 상의 질량 분율을 계산하였으며22), 이어서 전체 Si의 전환율(XSi)과 α-Si3N4, β-Si3N4 의 분율(Xα, Xβ)을 구하였다. 구체적인 계산과정은 피크강도 비를 이용해 상분율(Wα, Wβ, WSi)을 산출한 뒤, 이를 변환식에 대입하여 산정하는 방식으로 진행하였다. 관련된 식은 아래 식(1), (2), (3), (4), (5), (6)에 정리하였다.
이후 최적 질화 조건을 도출하기 위하여, 100% 질화율이 달성된 시료를 대상으로 입도분석(PSA)과 주사전자현미경(SEM) 분석을 수행하였다.
3. 결과 및 토의
3.1 회수 실리콘의 물리ㆍ화학적 특성
재활용 공정을 거쳐 폐모듈로부터 회수된 실리콘의 Si3N4 합성 원료 적합성을 평가하기 위해 우선적으로 화학적 순도와 물리적 특성을 확인하였다. 특히 불순물의 존재는 질화 반응 속도 및 상분율에 직접적인 영향을 미치므로, 순도 검증은 후속 실험을 위한 필수 단계라 할 수 있다. 본 연구에서는 회수된 실리콘을 볼밀링하여 미세 분말화한 뒤 ICP-OES분석을 통해 분말의 순도를 확인하였다.
Table 2.
Purity of ball-milled recycled silicon powder after 2-step acid etching analyzed by ICP-OES
| Sample name | Element (ppm) | Purity (%) | |||||||
| Al | Ag | Ti | Sn | Pb | Cu | Zn | Fe | ||
| Recycled Si | 46.5 | 177.0 | 33.2 | 47.5 | 54.0 | 5.9 | 10.0 | 12.4 | 99.96 |
분석원소는 Table 2에 제시한 바와 같이, 모듈 및 재활용 공정 과정에서 혼입될 수 있는 주요 불순물 8가지이다. Al과 Ag는 각각 후면 및 전면 전극에서 기인한 불순물이며, Ti는 PET계열 백시트에 함침되어 있던 TiO2의 형태로 혼입된 불순물이다. Cu, Pb, Sn은 구리 리본을 구성하는 물질이며, Zn과 Fe는 분쇄과정 중 장비로부터 혼입될 수 있는 불순물로, 해당 8가지 원소를 대표 불순물로 선정하여 분석을 진행하였다. 분석결과 r-Si의 순도는 99.96%로, 불순물 원소는 수십 ~ 수백 ppm정도로 낮게 잔존하여 불순물이 효과적으로 제거되었음을 알 수 있었다. 다만, 일부 잔여하는 불순물이 존재하는 이유는 분쇄과정 중에 발생하는 응집에 의해 제거되지 못한 것으로 판단된다18). 또한 Ag와 Cu의 경우 에칭과정에서 사용된 염산과의 반응성이 낮으며 질산에 반응하는 물질인데17), Cu의 경우는 체질과정에서 일차적으로 제거 후 질산과 반응하기에 미량만 잔여하였으나, Ag의 경우 사전에 제거되는 것 없이 질산에만 반응하였기에, 비교적 다량 잔류한 것으로 판단된다. 한편, Ti의 경우 TiO2 형태로 존제하는데, TiO2는 화학적으로 매우 안정적이어서 산과의 직접적인 반응은 거의 일어나지 않으나23), 산처리 이후 중화하는 과정에서 물리적으로 제거된 것으로 판단된다. 이러한 결과는 r-Si가 Si3N4 합성원료로 활용가능한 수준의 순도로 확보되었음을 의미한다.
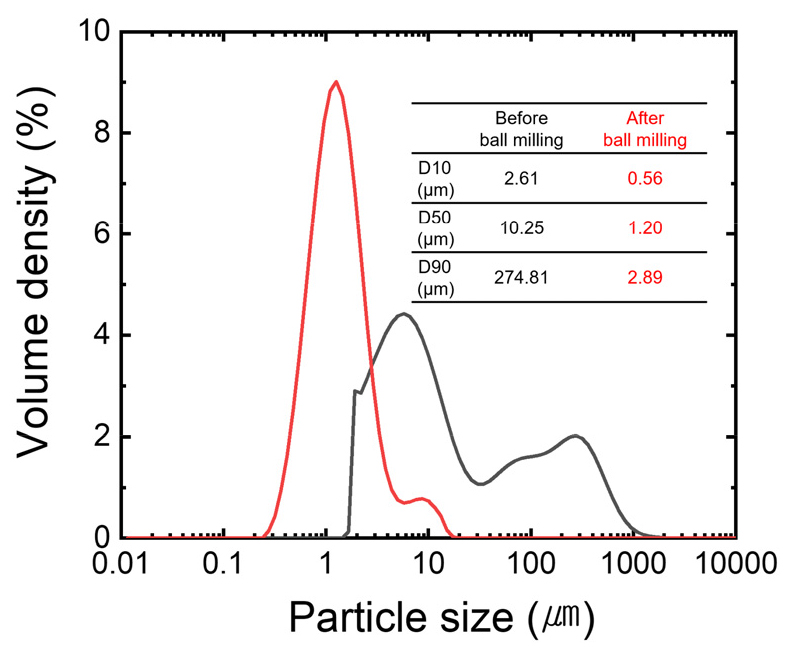
Fig. 1은 볼밀링 전후의 r-Si 분말 입도 분포 변화를 나타낸 것이다. 파쇄(crushing)만 거친 시료의 경우 D50 입도는 약 10.25 µm 수준이었으며, D90은 274.81 µm로, 100 µm를 초과하는 거대 입자가 다수 존재함을 확인하였다. 파쇄 장비인 로터리 커터밀은 내부의 회전 블레이드와 고정 블레이드 사이의 맞물림 작용을 통해 시료를 절단하는 방식으로 이루어진다. 그러나 이러한 파쇄 과정은 균일하게 일어나지 않아, 일부 입자는 반복되는 충격과 전단력에 의해 미세하게 파쇄되는 반면, 다른 입자들은 절단 과정에서 응집되거나 파쇄되지 못한 덩어리 상태로 장비를 빠져나와 충분히 파쇄되지 못한다. 그 결과, 미세 입자와 거대 입자가 공존하는 쌍봉(bimodal) 분포가 형성되며, 특히 100 µm를 초과하는 거대 입자의 존재는 로터리 커터밀 기반 파쇄 과정에서 발생하는 이러한 불균일성을 잘 보여준다. 볼밀링을 적용한 결과, D50은 1.20 µm로 급격히 감소하였으며, D90 또한 2.89 µm로 줄어들어, 볼밀링 전 존재하던 큰 입자들이 적절하게 밀링되었음을 확인할 수 있었다. 이때, 직경 10 mm 볼은 큰 입자를 분쇄하는데 주로 기여하였고, 직경 3 mm의 소형볼이 작은 입자를 추가적으로 분쇄하여 분포를 균질화 하는 역할을 하였다24). 결과적으로, Si3N4 합성에 요구되는 최적의 입도(1 µm)의 실리콘 분말을 확보할 수 있었다25).
Fig. 2는 볼밀링 전후의 r-Si 분말의 표면 미세구조를 SEM으로 관찰한 결과이다. (a), (b) 이미지는 볼밀링 전의 분말 형상을, (c), (d)이미지는 볼밀링 후의 이미지를 나타낸것이다. (a), (c)는 ×300배율 이미지, (b), (d)는 ×5000배율의 이미지이며, 이는 동일한 배율로 직관적인 입자크기 비교를 위해 균일한 배율을 배치하였다. 파쇄만 거친 시료의 경우 수십 ~ 수백 µm에 달하는 다양한 입도의 불규칙한 다각형입자들이 관찰되었으며, 입자표면은 분쇄 중 발생한 파괴면이 나타났다. 반면 볼밀링을 적용한 시료는 수 µm 이하의 미세입자들이 균일하게 분산되어 있는 모습을 보였으며, 입자형상은 다각형 형태를 유지하는 것을 확인할 수 있었다. 이러한 결과는 볼밀링 과정에서 큰 입자가 반복적인 충격을 통해 효과적으로 분쇄되었으며, 균일한 입도분포를 가지는 r-Si 분말을 확보하였음을 반증한다. 또한 앞서 제시한 입도 분석 결과와도 일관성을 갖는다.
3.2 질화 반응 거동 및 Si3N4 합성결과
볼 밀링 과정을 통해 균일한 입도 분포를 확보한 r-Si 분말은, 이후 여러 열처리 조건에서의 질화 실험을 통해 Si3N4 합성 반응 거동을 평가하였다.
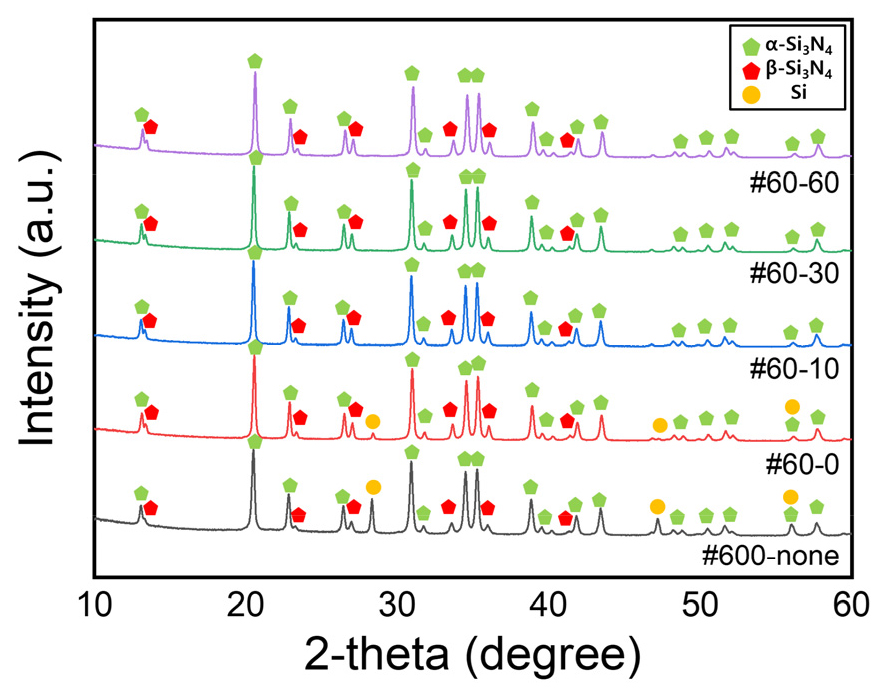
Fig. 3은 서로 다른 열처리 조건에서 합성된 Si3N4의 XRD패턴을 나타낸 것이다. #600-none 시편의 경우 10시간이라는 장시간동안 1350℃에서 열처리를 진행했음에도 Si peak가 뚜렷하게 관측되었다. 이는 시편 내부에 미반응한 Si이 잔여하는 것으로 판단된다. 반면 1350℃에서 1 h 유지 후 1450℃로 승온시킨 나머지 4개의 샘플에서는 비교적 짧은 시간 유지했음에도 Si의 peak가 현저하게 감소되거나 소멸하였으며, 1450℃ 장시간 유지조건에서도 α-Si3N4가 주상으로 형성됨을 확인할 수 있었다. 정량적 전환율 및 반응속도와 관련된 논의는 Fig. 4와 함께 제시하였으며, 각 상(α, β)의 상대적 분율의 변화는 Fig. 5에서 보다 구체적으로 논의하였다.
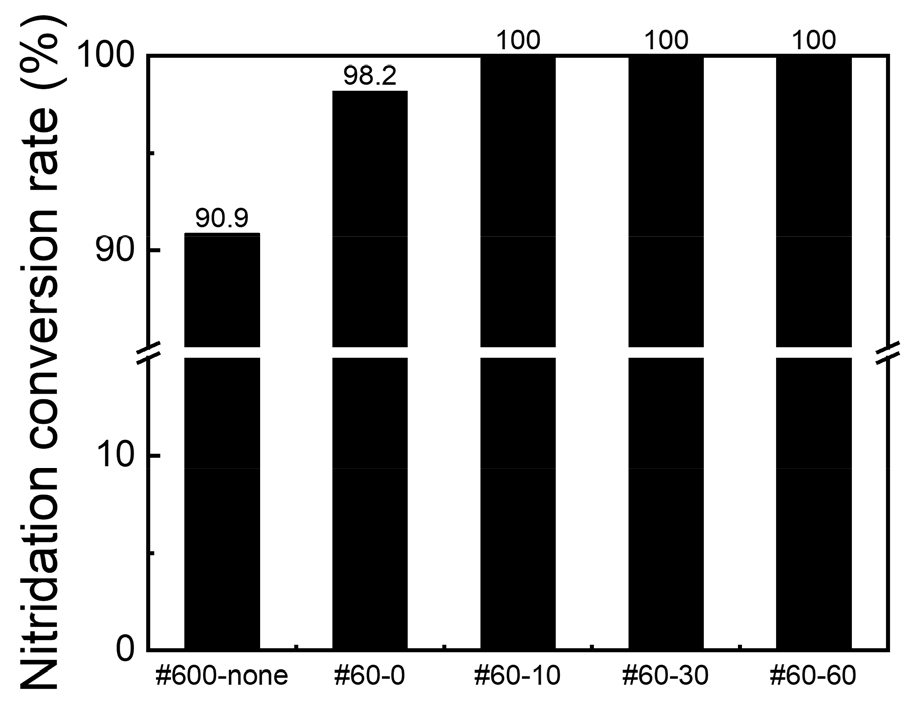
Fig. 4는 각 시편의 Si에서 Si3N4로의 전환율을 나타낸 그래프이다. 전환율은 앞서 제시한 계산식에 따라 산출되었다. 1350℃에서 장시간 유지한 #600-none 시편은 전환율이 90.9% 수준에 머물러, 고체상 확산 기반 반응의 속도론적 한계를 드러냈다. 이는 Jennings 등이 제시한 바와 같이26), 실리콘의 융점 이하 조건에서는 Si표면에 Si3N4 피막이 두껍게 형성되며, 이후 반응은 질소 확산에 의해 지배되어 반응 속도가 급격히 저하되는 Diffusion 지배단계로 전환되었기 때문이다. 그러나 1350℃에서 1 h 전처리 후 1450℃로 승온한 시편들은, #60-0을 제외하면 모두 100% 전환율을 달성하였다. 특히 #60-10 시편은 단 10 min의 1450℃ 유지에도 완전 질화가 이루어져, 전처리와 고온 조건의 결합이 반응 균일성과 효율성을 크게 향상시켰음을 보여준다. 이는 Si이 1414℃ 이상에서 용융됨에 따라 고체상태에서 지배적이던 표면확산 제약이 사라지고, 액상 Si과 N2 간의 직접반응이 가능해지는 동시에, 질소의 확산속도 또한 크게 증가되어 반응성이 급격히 증가했기 때문이다26). 실제로 Yang et al. (2022)27)의 연구에서는 1500℃에서 용융된 실리콘의 질화 속도가 1350℃의 고체 실리콘 대비 약 109배 이상 빠르다고 보고되어, 본 연구에서 관찰된 고온 조건의 급속 질화 경향을 잘 뒷받침한다.
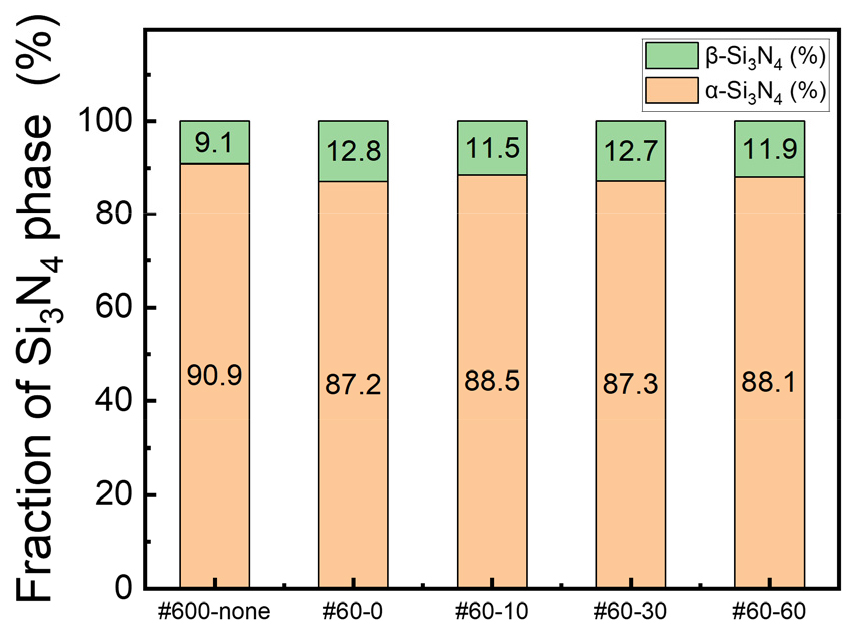
Fig. 5는 서로 다른 열처리 조건에서 합성된 시편의 α-Si3N4와 β-Si3N4의 상분율을 나타낸 것이다. 모든 시편에서 α-Si3N4가 우세하게 형성되었으며, 그 비율은 약 87–91% 수준으로 관찰되었다. 반면 β-Si3N4 분율은 9-13%범위에 머물렀으며, 열처리 유지시간이 증가하더라도 뚜렷한 증가 경향성은 나타나지 않았다. #600-none 샘플의 경우 Si의 융점(1414℃) 이하인 1350℃에서 반응을 진행하였기에 대부분 고상반응으로 반응이 진행이 되어 α-Si3N4상이 주상으로 도출되었다. 다른 조건의 시편들에서도 α상이 우세하게 형성되었는데, 이는 내부에서 용융이 발생하더라도 β 상으로의 전환온도인 약 1500℃에는 미치지 못했기 때문으로 판단된다25). 한편, 내부 상이 증가함에 따라서 β 상 또한 지속적으로 증가한 것으로 판단되는데, 이는 주로 표면 산화막에서 기인한 SiO의 기상 반응과 산소의 산화/환원 사이클을 통해 형성된 것으로 판단된다. 특히, Si의 융점이상으로 승온된 시편에서는, 그렇지 않은 시편에 비해 β-Si3N4 분율이 일부 증가하는 경향이 확인되었다. 이는 용융된 내부 Si에서 Si증발로 인해 SiO의 생성이 촉진되고, 이어서 SiO와 N2의 기상반응이 일어나면서 β 상의 분율이 일부 증가한 것으로 해석된다28). 자세한 메커니즘 및 화학식은 3.3절에서 논의하였다.
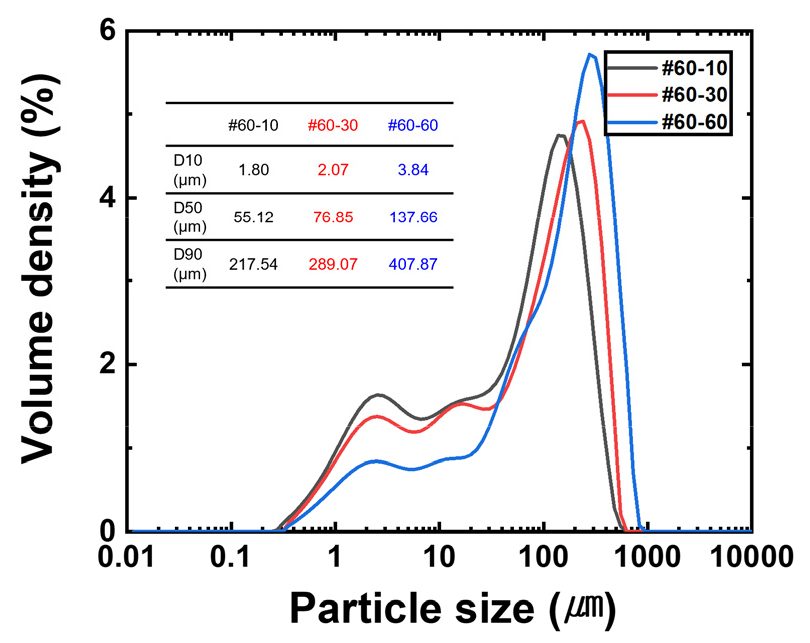
Fig. 6은 질화반응이 완전히 진행된 Si3N4 시편(#60-10, #60-30, #60-60)의 입도 분포를 나타낸 것으로, 최적 반응시간 선정을 위해 비교하였다. PSA 결과, 모든 시편에서 쌍봉 분포 형상이 관찰되었는데, 1 µm 부분의 피크는 볼밀링으로 조절된 r-Si원료의 초기 입도특성을 그대로 반영하는 반면, 수십 ~ 수백 µm부분의 큰 피크는 질화과정에서 입자 조대화로 새롭게 형성된 것이다. 이러한 조대화는 고온 유지 시간이 증가할수록 뚜렷해졌으며, 이는 기존 연구에서 보고된 소결 시간 증가에 따른 입자 성장 경향과 일치한다29). 특히, 조대한 입자는 고온을 유지하면서 입자 성장뿐만 아니라, 질화 과정 중 발생할 수 있는 분말의 국소적인 용융으로 인한 모세관력(capillary force)으로 인해 입자간의 응집과 재배열을 유도하면서 형성된 것으로 해석된다. 액상 브리지(liquid bridge)에 기인한 이러한 모세관력은 인접 입자들을 끌어당겨 집합체 형성을 가속화한다30). 국소 용융 형성메커니즘은 3.3절에서 논의하였다. 일반적으로 입자 크기가 작은 것이 후속 공정에서 소결체의 치밀도 확보 측면에서 유리하기에31), 상대적으로 작은 입자 크기를 가지며, 공정 시간이 짧은 #60-10 조건이 최적의 공정 조건으로 판단된다.
이러한 경향성은 Fig. 7의 SEM 이미지를 통해 확인할 수 있었다. 일반적으로 α-Si3N4는 short rod 또는 equiaxed형태로 나타나는 반면, β-Si3N4는 비등방적 결정 성장을 통해 길게 뻗은 whisker 형상을 보이는 것으로 알려져 있다29). 모든 시편에서 이 두 가지 상이 혼재된 유사한 형상이 관찰되었으며, 이는 질화 시간이 달라지더라도 두 상이 큰 변화 없이 공존함을 의미한다. 또한 저배율 관찰 결과, 고온 유지 시간이 증가할수록 전체 입자의 크기가 점차 커지는 경향을 확인하였는데, 이는 장시간 질화 조건에서 입자 성장 및 조대화가 진행됨을 시사한다. 이러한 SEM 관찰 결과는 PSA 분석 결과와도 일치한다.

Fig. 7
Low-magnification (×800) and high-magnification (×10k) SEM images of Si3N4 powders synthesized under different holding times, (a) #60-10, (b) #60-30, (c) #60-60. The top left images show overall particle morphology, while the magnified views highlight the coexistence of equiaxed/short rod-like α-Si3N4 and whisker-like β-Si3N4
3.3 질화 반응 메커니즘 고찰
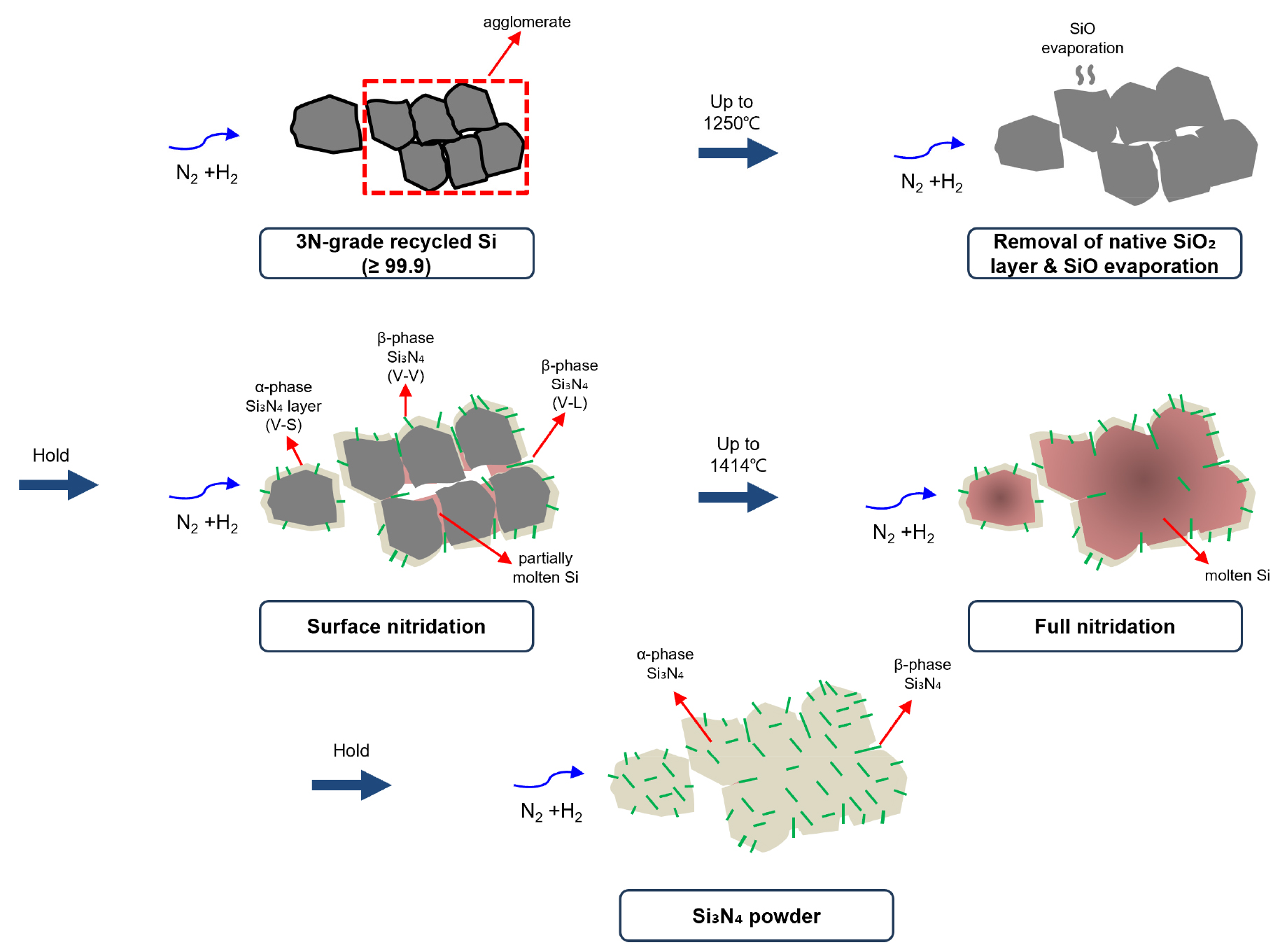
Fig. 8은 실리콘의 질화 반응 과정을 단계적으로 모식화하여 나타낸 것이다. 초기 실리콘 입자의 표면은 자연 산화막(SiO2)으로 덮여 있으며, 이는 질소의 확산을 억제하여 직접적인 반응을 방해한다. 이 산화막은 식(7), (8)과 같이 수소환원 또는 고온에서 Si와의 반응을 통해 제거된다.
식(7)의 경우 혼합가스 중 수소에 의해 SiO(g)가 생성되며32), 식(8)의 경우 1250℃ 이상에서 자연산화막에 의해 Si이 SiO로 휘발될 수 있음을 설명한다33).
산화막이 제거된 표면에서는 먼저 실리콘과 질소가 직접 반응하는 기상-고상(V-S)반응이 일어나 얇은 α-Si3N4 피막을 형성한다. 이때, 형성된 피막은 다공성 구조를 가지며, 이후 질소의 확산경로로 작용한다20). 다음으로, 국부적으로는 실리콘의 용융으로 생성된 액상이 기상–액상(V–L) 반응이 있다. 이 반응은 실리콘의 전체 온도가 융점 이하인 경우에도 일어날 수 있다. 질화 반응에서 발생하는 발열로 인해 응집체 및 입자 접촉부의 온도가 국부적으로 1500℃ 이상까지 상승하여 이로 인해 국부적인 용융이 일어날 수 있다34). 생성된 액상 Si은 기본적으로는 질소와 반응하여 α-Si3N4가 생성되지만, 1500℃이상에서 β-Si3N4으로 상변화가 일어날 수 있다. 마지막으로, 산화막에서 발생한 SiO(g) 기상종은 질소와 직접 반응하는 기상–기상(V–V) 반응을 통해 반응식 (9)와 같이 β-Si3N4를 형성할 수 있다35).
이후 Si의 용융온도(1414℃) 이상으로 승온하게 되면 분말내부에 잔여하던 Si이 용융된다. 다공성 α-Si3N4 피막을 통과하여 질소와 반응하는 Si은 1500℃ 이하 조건에서 α 상이 우선적으로 형성된다. 동시에 질화과정중 생성된 SiO가 산화·환원 과정을 거치며 분말 내부에서 지속적으로 재생성되는데, 대표적으로
와 같은 반응을 통해 β-Si3N4가 형성된다. SiO(g)는 N2와 반응하여 β-Si3N4를 생성하는 과정에서 O2를 생성하게 된다. 이중 일부 O2는 반응식 (10)처럼 다시 SiO(g)를 만드는데 기여하고 질화규소로 재합성되는 순환이 일어나 지속적으로 내부에 β 상이 형성되도록 한다36). 따라서, 질화가 완료된 분말은 내·외부 모두 α상과 β상이 혼재된 구조를 보이게 된다.
4. 결 론
본 연구에서는 폐 태양광 모듈로부터 회수한 실리콘 분말을 원료로 활용하여 고부가가치 Si3N4 소재 합성을 시도하였다. 회수된 실리콘은 불순물 제거 및 정제 과정을 거쳐 99.96% 라는 순도를 확보하였으며, 후속 공정의 반응성을 향상시키기 위해 볼 밀링을 통한 미세화 처리를 수행하여 D50 1.2 µm의 Si 분말을 확보하였다. 전처리된 분말은 XRD, SEM, PSA 등의 분석을 통해 물리ㆍ화학적 특성을 수행하였다. Si의 융점이상의 고온 질화 공정을 통해 1450℃ 10분 이상 유지 시편에서 질화율 100%를 달성하였으며, 상분석 결과 α-Si3N4이 87%이상 주상으로 형성되고 β-Si3N4는 국부 용융 및 기상 반응으로 소량 생성되었다. 또한 1450℃ 유지 시간이 길어질수록 입자 성장이 촉진되어 평균 입도가 증가하는것을 확인할 수 있었다. 최종적으로 최적 공정조건은 짧은 공정시간과 작은 입자 크기를 보인 #60-10 조건으로 도출되었다. 본 연구는 폐 모듈에서 회수한 실리콘을 고부가가치 Si3N4 세라믹으로 전환할 수 있는 실질적 재활용 경로와 최적 공정 조건을 제시하였다는 점에서 자원순환 및 친환경 소재 생산에 기여할 수 있을 것으로 기대된다.