1. 서 론
2. 실험 방법
3. 결과 및 고찰
4. 결 론
1. 서 론
지구온난화가 가속됨에 따라 신재생에너지에 대한 연구가 활발히 진행되고 있는 가운데 그 중 태양광 에너지는 가장 주목 받는 에너지이다. 이에 따라 태양광 에너지는 세계적으로 매년 꾸준한 성장세를 보이고 있다. 그러나 이러한 태양광 에너지도 기대 수명이 존재한다. 태양광 발전에 사용되는 태양광 모듈의 수명은 20-30년으로 다양하고 많은 양이 1990년대에 설치되어 이에 따라 많은 양의 태양광 폐모듈이 급증할 것으로 예상된다. IRENA 보고서에 따르면 2030년에 약 800만 톤, 2050년에 약 7천800만 톤의 태양광 폐모듈이 발생할 것으로 예상하고 있다1). 이러한 태양광 폐모듈을 처리하기 위해서 유럽 연합(European Union, EU)은 2012년부터 전기·전자 폐기물 처리 지침(Waste Electrical and Electronic Equipment, WEEE)을 통해 태양광 모듈을 전기·전자 폐기물로 지정하여 재활용하도록 개정하였다2). 국내의 경우 2023년 태양광 폐모듈에 대한 생산자책임재활용제도(Extended Producer Responsibility, EPR)를 시행하기로 합의 하였으며 이에 따라 태양광 폐모듈을 재활용하기 위한 기술 개발의 필요성이 증가하고 있다3).
태양광 모듈의 구성요소 중 하나인 태양전지의 경우 실리콘을 기반으로 은(Ag)과 알루미늄(Al)으로 이루어진 전·후면 전극, 반사방지막(Silicon Nitride, SiNx), 에미터(Emitter) 및 후면전계(Back Surface Field, BSF)로 이루어져 있다. 전과정 평가(Life Cycle Assessment, LCA)를 통해 태양전지 제작 시 원료 채취 과정에서 환경에 미치는 영향을 평가하였을 때 태양전지 내 Ag가 m2 당 가장 높은 지구 온난화 지수(Global Warming Potential, GWP)를 갖고 그 뒤를 실리콘이 잇는 것으로 보고되었다4). 또한 Ag는 가장 고가의 물질이기 때문에 이를 효과적으로 회수하여 재활용 할 수 있다면 경제적 및 환경적으로 큰 가치를 창출 할 수 있다5).
태양전지로부터 Ag를 회수하기 위해 많은 연구가 진행되고 있다. 태양전지로부터 Ag를 회수하기 위해서는 유기산을 이용하는 방법6) 및 무기산을 이용하는 방법7,8,9,10,11,12,13,14,15,16,17,18,19)이 있다. 유기산을 이용하는 방법의 경우 유기산의 높은 비용 및 긴 공정 시간 등으로 인해 태양광산업에 적용하기 어렵다는 단점이 있다. 무기산을 이용하는 방법의 경우 일반적으로 질산(Nitric acid, HNO3)을 이용하여 Ag를 침출시킨다. 하지만 이는 공정 중 발생하는 아산화 질소가스(Nitrous Oxide gas, Nox gas)로 인해 환경오염을 유발시키는 단점이 있다20,21,22). 또한 HNO3 용액의 경우 0단계에서 4단계로 이루어진 NFPA (National Fire Protection Association)지수 중 신체에 미치는 유해 정도가 4단계로 매우 높은 독성을 지니고 있는 것을 확인할 수 있다. 이와 같은 이유로 HNO3 를 대체 할 수 있는 용액의 개발이 필요한 사항이다.
태양전지 내 반사방지막 층(Silicon Nitride layer, SiNx layer)의 경우 일반적으로 불산(Hydrofluoric acid, HF)용액을 사용하여 제거하는데 이는 HNO3 와 같이 매우 높은 독성을 지니며 또한 국내 허용 배출가스 기준이 3 ppm23) 수준으로 환경규제가 매우 심한 편이다. 이러한 문제점을 해결하기 위해 HF 용액을 사용하지 않고 반사방지막 층을 제거하는 연구사례가 있다24). 해당 연구 사례의 경우 반사방지막을 제거하기 위해 HF 용액이 아닌 플루오린화 나트륨(Sodium fluoride, NaF)가 첨가된 황산(Sulfuric acid, H2SO4) 용액을 사용하였다.
따라서 본 연구에서는 HNO3 용액을 사용하지 않고 태양전지 내 Ag 전극의 제거가 가능하며 동시에 반사방지막 층 까지 제거가 가능한 공정을 개발하였다. H2SO4와 과산화수소(Hydrogen peroxide, H2O2)를 조합한 혼합 용액에 NaF를 첨가하여 Ag를 침출 시키는 동시에 반사방지막 또한 제거 하였다. 침출 공정에서 가장 주요한 용액의 농도를 제어하여 최적 공정을 확보하였고 이를 종래의 HNO3 침출 공정과 비교 하였다. 상기 용액의 경우 HNO3와 HF 용액에 비해 비교적 낮은 독성을 가지며 공정 중 발생된 가스로 인해 환경오염의 문제가 없는 것으로 확인되었다.
2. 실험 방법
본 논문에서는 NaF가 첨가된 H2SO4와 H2O2 혼합용액을 사용하여 Ag 전극 및 반사방지막 층을 제거하였다. 예비 실험을 통해 H2SO4 와 H2O2 용액의 혼합 비율 1:1, 첨가제 1 몰랄농도(molality, m), 중량 고액비 20, 공정 온도 50℃, 공정 시간 20분으로 고정하였으며 교반 속도는 120 RPM으로 진행하였다. 사용된 H2SO4, H2O2 혼합 용액의 농도에 따른 Ag 침출 효과를 확인하기 위해 농도를 실험 변수로 두어 진행하였으며 적용한 화학 공정 조건은 Table 1에 나타내었다.
Table 1
Experimental concentrations in each etching process
|
Sample
|
Solution
|
Additive
|
Solid-liquid ratio
|
Temperature
|
Time
|
|
A
|
H2SO4 10 wt%
|
H2O2 10 wt%
|
NaF (1 m)
|
20
|
50℃
|
20 min
|
|
B
|
H2SO4 15 wt%
|
H2O2 15 wt%
|
|
C
|
H2SO4 20 wt%
|
H2O2 20 wt%
|
|
D
|
H2SO4 25 wt%
|
H2O2 25 wt%
|
|
E
|
H2SO4 30 wt%
|
H2O2 30 wt%
|
|
F
|
HCl 36 wt%
|
-
|
30℃
|
|
G
|
H2SO4 30 wt%
|
H2O2 30 wt%
|
NaF (1 m)
|
50℃
|
H2SO4, H2O2 혼합 용액의 농도를 변경하여 Ag 전극 및 반사방지막을 제거하였으며 공정의 농도 별 Ag 침출 효과를 확인하기 위해 30 wt% HNO3를 이용해 Ag 전극을 침출시킨 대조군과 비교하였다. 이 때 침출 효과는 유도 결합 플라즈마 원자방출분광기(Inductively Coupled Plasma-Atomic Emission Spectroscopy, ICP-AES, Optima5300DV, Perkin Elmer, USA)분석을 진행하여 침출 액 내에 존재하는 Ag의 농도를 통해 확인하였다.
한편 공정 중 부반응에 의해 회수 스크랩 내 침전물이 발생하였고 이를 X선 회절 분석법(X-ray Diffraction, XRD, DMAX-2500, Rigaku, Japan) 분석을 통해 화학 구성물을 확인하였으며 HSC Chemistry 프로그램을 이용하여 열역학적 해석을 진행하였다. 이는 공정 중 태양전지 내 Al전극에 의해 발생되는 부반응으로 이를 제어하고자 반응 전 태양전지로부터 Al전극을 선행적으로 제거하는 공정을 수행하였으며 이에 대한 개략도를 Fig. 1에 나타내었다.
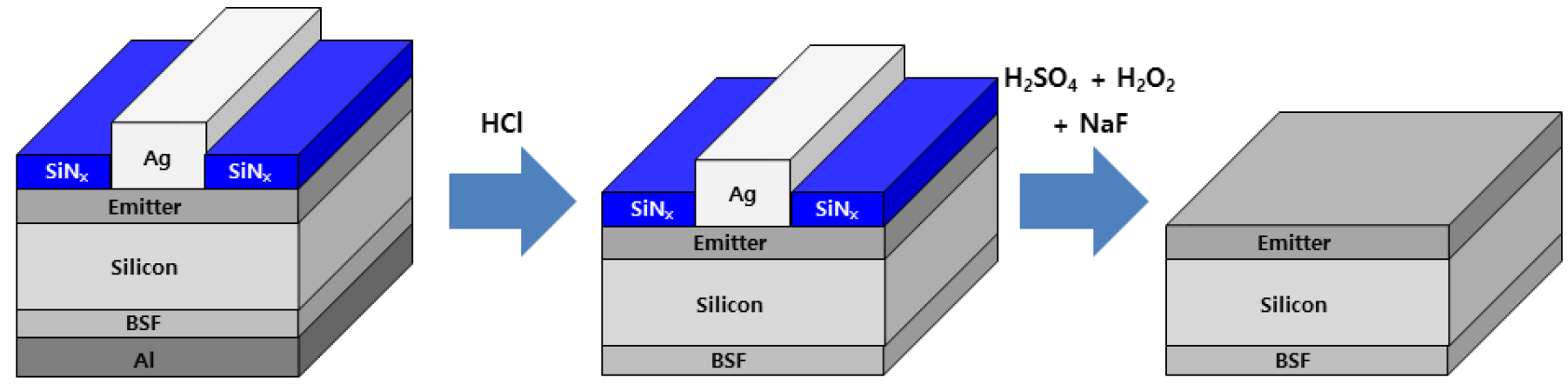
Fig. 1
Schematic diagram of the process of removing layers from the solar cell surface
염산(Hydrogen chloride, HCl)을 이용하여 Al전극을 제거하였고 이후 NaF가 첨가된 H2SO4, H2O2 혼합 용액을 통해 Ag 전극 및 반사방지막을 제거 하였다. NaF가 첨가된 H2SO4, H2O2 혼합 용액의 경우 Ag 침출이 가장 효과적인 농도 30 wt%를 이용하였으며 적용한 화학 공정 조건은 Table 1에 나타내었다.
공정 후 Ag 침출 효과를 확인하기 위해 ICP-AES 분석을 진행하여 침출액 내 Ag농도를 대조군과 비교하였고 주사전자현미경(Scanning Electron Microscope, SEM, S-4800, Hitachi, Japan)/에너지 분산 X선 분광법(Energy Dispersive X-ray Spectroscopy, EDS, S-4800, Hitachi, Japan) 분석을 통해 회수 스크랩 내 Ag제거 여부를 확인하였다.
3. 결과 및 고찰
혼합 용액을 이용한 침출 공정 후 Ag 전극의 경우 용액의 농도가 증가됨에 따라 반응성이 상승하는 것으로 확인되었고 반사방지막의 경우 모든 농도에서 제거가 가능한 것으로 확인되었다. Fig. 2에 혼합 용액 농도에 따른 Ag 전극 및 반사방지막의 제거 거동을 나타내었다.

Fig. 2
The dissolution behaviors of Ag electrodes, SiNx layers according to H2SO4 + H2O2 mixture concentration of A, B, C, D, E samples
Ag 전극의 경우 H2O2와 H2SO4 용액의 농도가 증가 할수록 반응성이 상승하는 거동을 나타냈다. 사용된 용액의 농도가 증가함에 따라 침출 효과가 상승하는 것으로 확인되어지며 보다 정확한 농도 별 Ag 침출 효과를 확인하기 위해 ICP-AES 분석으로 침출액 내 Ag 농도를 비교하였다. 반사방지막의 경우 위 그림을 보았을 때 모든 조건에서 반사방지막이 제거 된 것으로 보아 모든 농도 조건에서 제거가 가능 한 것으로 보아진다. 농도 별 Ag 침출 효과를 비교하기에 앞서 태양전지 내 존재하는 Ag의 양을 확인하기 위해 30 wt% HNO3으로 Ag를 완전 침출 시켜 ICP-AES 분석을 진행한 결과 용액 내 Ag농도는 145 ppm으로 확인되었다. 이에 따라 해당 결과를 대조군으로 두어 H2SO4, H2O2 혼합 용액 농도 조건에 따른 Ag 침출 효과를 비교하였으며 이를 Fig. 3에 나타내었다.
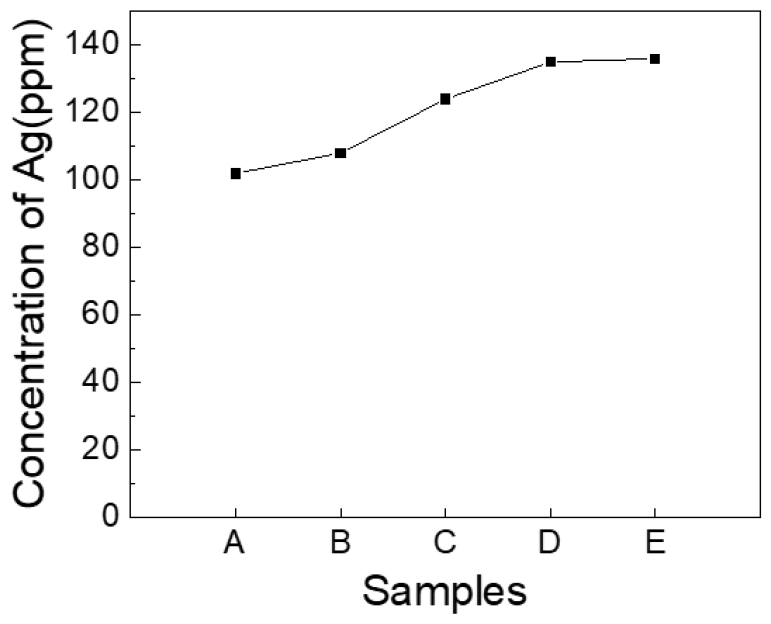
Fig. 3
Ag concentration in the chemical solution measured by ICP-AES
분석 결과 10 ~ 30 wt% 농도 조건에서 검출 된 Ag 양은 각각 102, 108, 124, 135, 136 ppm으로 나타났다. Ag 전극의 경우 반응식(1)과 같이 H2SO4와 H2O2에 의해 이온화 되어 제거된다25). 분석 결과를 보았을 때 A, B, C 샘플의 경우 Ag를 이온화 시킬 SO42- 및 OH-가26,27) 부족하여 낮게 검출 된 것으로 판단되고 반면 결과 값이 상대적으로 높게 검출 된 샘플 D와 E의 경우 Ag를 이온화하기 위한 SO42-, OH-가 충분한 것으로 보아진다. 특히 샘플 E의 결과 값이 대조군과 가장 비슷한 수치를 나타내는 것으로 보아 Ag 전극을 전부 제거하기 위해서는 농도 30 wt%가 필요한 것으로 판단된다. 반사방지막의 경우 반응식(2)와 같이24) 용액 내 H+ 및 F-에28,29,30) 의해 이온화 되어 제거되는데 Fig. 2 결과를 보아 H2SO4 용액의 모든 농도 조건에서 제거가 가능한 것으로 나타났다. 한편 공정 중 부반응으로 인해 형성된 것으로 예상되는 물질이 회수 스크랩 내 잔존하는 것을 확인하였으며 이를 Fig. 4에 나타내었다.

Fig. 4
Picture of substances formed by side reactions
위 그림과 같은 물질이 공정 후 회수한 스크랩 내 잔존할 경우 Ag, Al 전극 및 반사방지막 제거 후 행해질 실리콘 회수 공정에 문제가 발생할 수 있어 이러한 현상을 억제할 필요가 있다. 따라서 해당 물질의 화학 구성물을 파악하기 위해 XRD분석을 진행하였고 그 결과를 Fig. 5에 나타내었다.
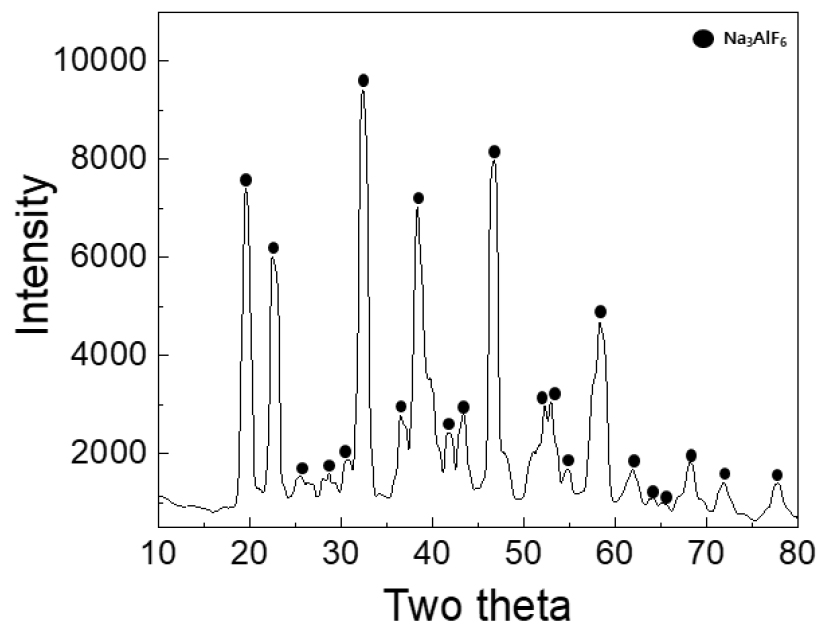
Fig. 5
XRD pattern of substances formed by side reactions
분석 결과 위 그림과 같이 Na3AlF6 (Sodium aluminium hexafluoride)가 검출되었다. 물질의 화학 구성이 Al과 Na, F로 이루어 진 것으로 보아 NaF와 태양전지 내 Al 전극에 의해 생성된 것으로 판단되어진다. 이에 대해 보다 정확하게 파악하기 위해 HSC Chemistry 프로그램을 이용하여 열역학적 해석을 진행하였으며 그 결과를 Fig. 6에 나타내었다.
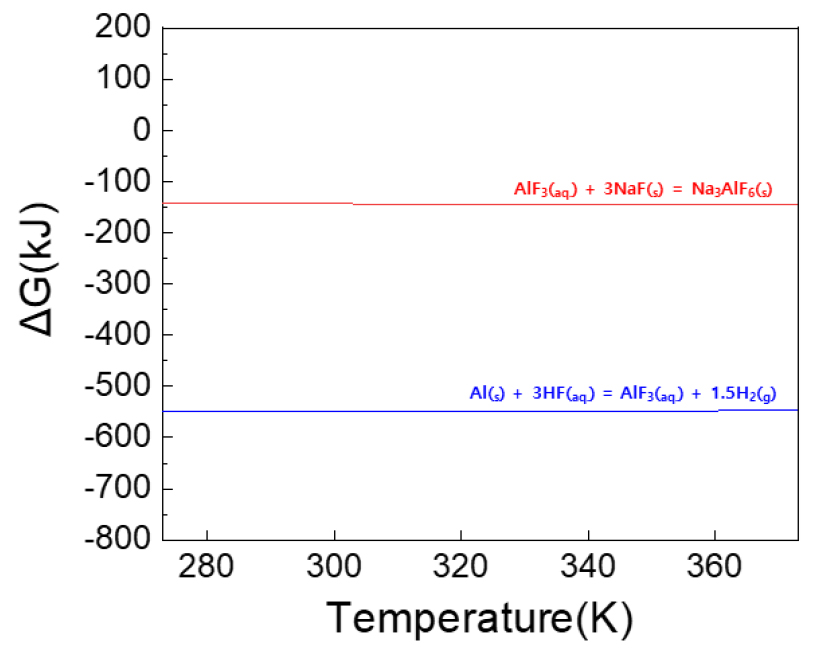
Fig. 6
ΔG(kJ) for reactions of Al with H2SO4 and NaF
해석 결과 태양전지 내 Al이 NaF와 H2SO4에 의한 부반응으로 Na3AlF6이 생성된 것으로 확인되었다. 결과적으로 스크랩 회수 측면에서 해당 현상을 제어할 필요가 있으며 이에 따라 NaF가 첨가된 H2SO4, H2O2 혼합 용액의 공정 전 Al 전극의 제거가 필요한 것으로 사료된다.
태양전지 내 Al 전극을 제거하기 위해 HCl 용액을 이용하였으며 사용된 조건은 농도 36 wt%, 고액비 20, 공정 온도 30℃, 공정 시간 20분이었다. 이후 샘플 F에 NaF가 첨가된 H2SO4, H2O2 혼합 용액을 통해 Ag 전극 및 반사방지막을 제거하였고 적용한 혼합 용액의 농도 조건은 Ag가 가장 효과적으로 침출된 30 wt% 조건을 적용하여 진행하였다. 공정 후 태양전지 내 Ag 전극, 반사방지막이 전부 제거가 되었으며 그 결과를 Fig. 7에 나타내었다.

Fig. 7
The dissolution behaviors of front surface according to each process of F: After HCl process, G: After NaF + H2SO4 + H2O2 process
반응식(3)과 같이 HCl 용액을 이용하여 태양전지 내 Al 전극을 이온화시켜 제거하였으며31) 이 후 NaF가 첨가된 H2SO4, H2O2 혼합 용액 공정을 진행한 결과 Ag 전극 및 반사방지막이 전부 이온화 되어 제거된 것으로 보아진다. Ag 전극의 경우 반응식(1)과 같이 용액 내 H2SO4 및 H2O2 로 인해 제거 되었으며 반사방지막 또한 반응식(2)와 같이 용액 내 NaF와 H2SO4에 의해 제거되었다. Al 전극이 제거된 후 반응이 진행됨에 따라 부반응이 발생하지 않아 반응 후 스크랩 내 Na3AlF6가 잔존하지 않은 것을 확인하였다. 이후 Ag 전극 제거 효과를 확인하기 위해 ICP-AES 분석을 진행하여 침출액 내 Ag 농도를 확인하였고 이를 Fig. 8에 나타내었다.
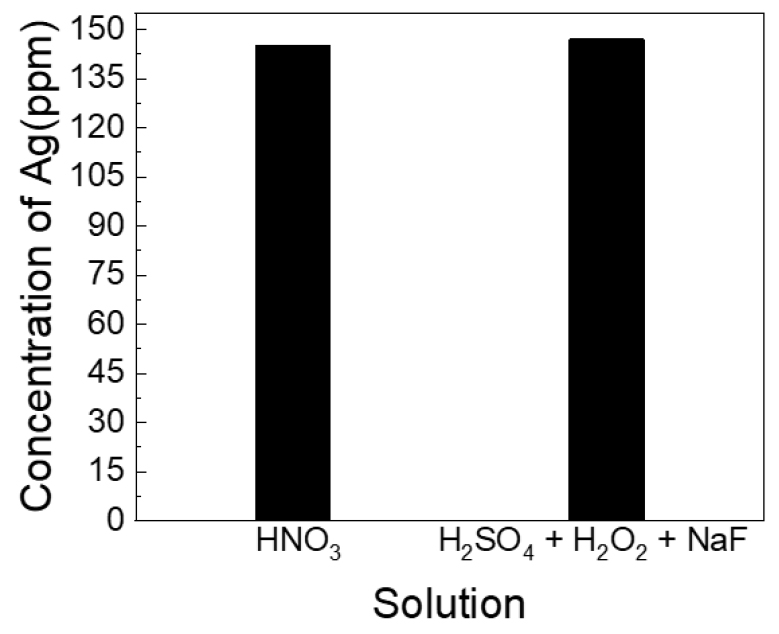
Fig. 8
Ag concentration in the chemical solution measured by ICP-AES
분석 결과 검출 된 Ag 양은 147 ppm으로 이는 태양전지 1개 내에 존재하는 Ag의 양과 동등한 수치인 것으로 보아 모두 침출되었다고 판단된다. 또한 이는 NaF가 첨가된 H2SO4, H2O2 혼합 용액이 HNO3 용액을 대체 할 수 있음을 의미한다. 해당 결과로 보아 태양전지 내 Ag 전극을 제거하기 위한 최적 농도는 30 wt%로 확인된다. 이 후 회수 스크랩 내 Ag 전극의 제거 여부를 확인하기 위해 SEM/EDS 분석을 진행하였으며 이를 Fig. 9에 나타내었다.
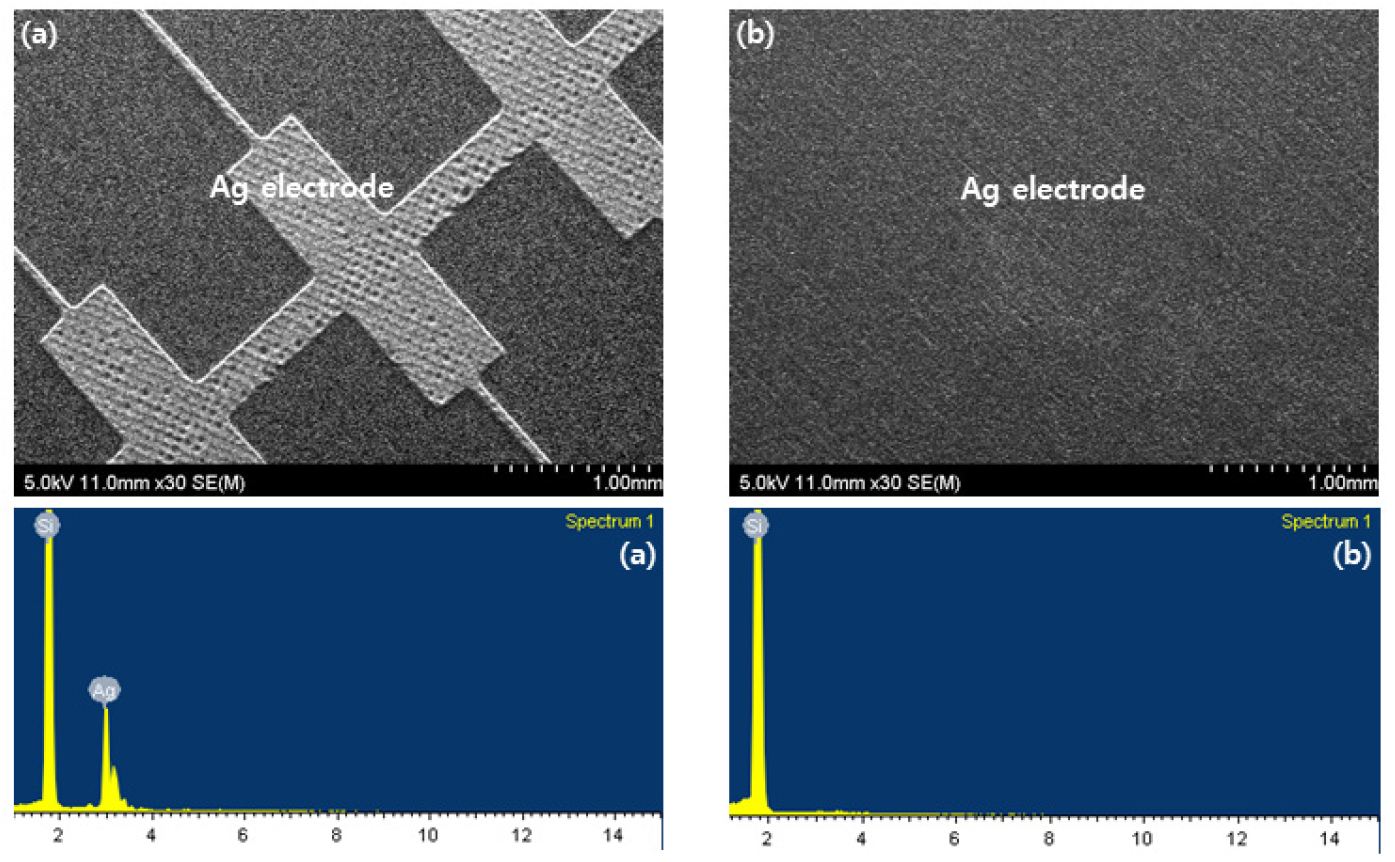
Fig. 9
SEM/EDS analysis of solar cell: Front surface Before etching process (a), Front surface after etching process (b)
SEM 이미지 확인 결과 반응 후 Ag 전극이 확인되지 않는 것으로 보아 NaF가 첨가된 H2SO4, H2O2 혼합 용액에 의해 Ag 전극이 전부 제거된 것으로 판단된다. 또한 EDS 분석을 통해 확인한 결과 Ag가 검출되지 않았음으로 공정 후 태양전지 내 Ag 전극이 전부 제거된 것으로 확인된다. 결과적으로 NaF가 첨가된 H2SO4, H2O2 혼합 용액의 농도가 30 wt%일 때 태양전지 내 Ag가 모두 제거 된 것으로 나타났으며 이는 HNO3용액을 대체 할 수 있는 수준으로 확인되었다.
4. 결 론
본 논문에서는 태양전지로부터 Ag 전극과 반사방지막을 제거하기 위해 NaF가 첨가된 H2SO4, H2O2 혼합 용액을 사용함에 있어 농도에 따른 Ag 침출 효과를 평가하였다. ICP-AES 분석을 통해 침출 효과를 확인하였으며 이를 HNO3 용액을 사용한 경우와 비교하였다. 분석 결과 사용된 용액의 농도가 증가함에 따라 침출 효과가 상승하는 거동을 나타내었고 30 wt% 조건에서 가장 효과적으로 침출된 것을 확인할 수 있었다. 태양전지 후면의 Al 전극이 용액 내 NaF와 H2SO4에 의한 부반응으로 침전물이 생성되어 이로 인해 HC1 용액을 이용하여 Al 전극을 선행적으로 제거한 후 Ag 침출 공정을 진행하였고 Ag 침출 공정에 사용된 용액의 농도는 Ag가 가장 효과적으로 침출된 농도 30 wt%를 적용하였다. 공정 후 ICP-AES 분석을 통해 침출액 내 Ag 양을 확인 했을 때 검출 된 수치는 147 ppm으로 이는 태양전지 한 개에 함유되어 있는 Ag의 양과 동등한 수준이었다. 또한 Al 전극의 제거가 선행되었음에 따라 공정 후 침전물이 발생하지 않은 것을 확인할 수 있었다. 이 후 SEM /EDS 분석을 통해 스크랩 내 Ag 전극의 제거 여부를 확인하였다. SEM 이미지 확인 결과 Ag 전극이 관찰되지 않았고 EDS 분석의 경우 Ag가 검출되지 않은 것으로 보아 태양전지 내 Ag 전극이 전부 제거 된 것으로 확인되었다. 반사방지막의 경우 공정 후 스크랩 표면을 육안으로 확인 한 결과 모두 제거 된 것으로 보아졌다. 결론적으로 태양전지 내 Ag 전극을 제거하기 위한 최적의 농도 조건은 30 wt%로 확인되었으며 이는 HNO3용액을 대체하기에 충분한 수준이었다. 또한 에미터 및 후면전계층을 제외 한 모든 구성 요소가 제거되었음에 따라 추가적인 공정을 통해 고순도의 실리콘을 회수할 수 있을 것으로 판단된다.
Acknowledgements
본 연구는 한국환경산업기술원 재활용저해제품 순환이용성 개선기술개발사업의 지원을 받아 수행한 연구 과제입니다(과제번호: RE202003052).
References
Stephanie, W., Wade, A., and Heath, G., End-of-life Management: Solar Photovoltaic Panels, 2016.
European Parliament, European Parliament and of the Council of 4 July 2012 on Waste Electrical and Electronic Equipment, WEEE, Official Journal of the European Union L, Vol. 197, No. 38, pp. 37-71, 2012.
Lee, K. and Cha, J., Management of Solar Photovoltaic Panels under the Extended Producer Responsibility Legislation, Journal of the Korean Society of Mineral and Energy Resources Engineers, Vol. 56, No. 4, pp. 367-376, 2019.
10.32390/ksmer.2019.56.4.367Maani, T., Celik, I., and J.Heben, M., Environmental Impacts of Recycling Crystalline Silicon (c-SI) and Cadmium Telluride (CDTE) Solar Panels, Science of The Total Environment, Vol. 735, pp. 138827, 2020.
10.1016/j.scitotenv.2020.13882732464407Markert, E., Celik, I., and Apul, D., Private and Externality Costs and Benefits of Recycling Crystalline Silicon (c-Si) Photovoltaic Panels, Energies, Vol. 13, No. 14, pp. 3650, 2020.
10.3390/en13143650Yang, E. H., Lee, J. K., and Lee, J. S., Environmentally Friendly Recovery of Ag from End-of-life c-Si Solar Cell using Organic Acid and Its Electrochemical Purification, Hydrometallurgy, Vol. 167, pp. 129-133, 2017.
10.1016/j.hydromet.2016.11.005Radziemska, K. E. and Ostrowski, P., Chemical Treatment of Crystalline Silicon Solar Cells as a Method of Recovering Pure Silicon from Photovoltaic Modules, Renewable Energy, Vol. 35, No. 8, pp. 1751-1759, 2010.
10.1016/j.renene.2009.11.031Radziemska, K. E., Ostrowski, P., and Drabczyk, K., Experimental Validation of Crystalline Silicon Solar Cells Recycling by Thermal And Chemical Methods, Solar Energy Materials and Solar Cells, Vol. 94, No. 12, pp. 2275-2282, 2010.
10.1016/j.solmat.2010.07.025Lee, C. H., Hung, C. E., and Tsai, S. L., Resource Recovery of Scrap Silicon Solar Battery Cell, Waste Management & Research, Vol. 31, No. 5, pp. 518-524, 2013.
10.1177/0734242X1347943323460539Yi, Y. K., Kim, H. S., and Tran, T., Recovering Valuable Metals from Recycled Photovoltaic Modules, Journal of the Air & Waste Management Association, Vol. 64, No. 7, pp. 797-807, 2014.
10.1080/10962247.2014.89154025122953Park, J. S. and Park, N. C., Wet Etching Processes for Recycling Crystalline Silicon Solar Cells from End-of-life Photovoltaic Modules, RSC Advances, Vol. 4, No. 66, pp. 34823-34829, 2014.
10.1039/C4RA03895ADias, P., Javimczik, S., and Benevit, M., Recycling WEEE: Extraction and Concentration of Silver from Waste Crystalline Silicon Photovoltaic Modules, Waste Management, Vol. 57, pp. 220-225, 2016.
10.1016/j.wasman.2016.03.01626980485Dávid, S., Hylský, J., and Vaněk, J., Methods for Recycling Photovoltaic Modules and Their Impact on Environment and Raw Material Extraction, Acta Montanistica Slovaca, Vol. 22, No. 3, pp.257-269, 2017.
Huang, W. H., Shin, W. J., and Wang, L., Strategy and Technology to Recycle Wafer-silicon Solar Modules, Solar Energy, Vol. 144, pp. 22-31, 2017.
10.1016/j.solener.2017.01.001Łażewska, A. K., Radziemska, E. K., and Sobczak, Z., Recovery of Silver Metallization from Damaged Silicon Cells, Solar Energy Materials and Solar Cells, Vol. 176, pp. 190-195, 2018.
10.1016/j.solmat.2017.12.004Yousef, S., Tatariants, M., and Tichonovas, M., Sustainable Technology for Mass Production of Ag Nanoparticles and Al Microparticles from Damaged Solar Cell Wafers, Waste Management, Vol. 98, pp. 126-134, 2019.
10.1016/j.wasman.2019.08.01931445457Wongnaree, N., Kritsarikun, W., and Ma-ud, N., Recovery of Silver from Solar Panel Waste: An Experimental Study, Materials Science Forum, Vol. 1009, pp. 137-142, 2020.
10.4028/www.scientific.net/MSF.1009.137Chen, W. S., Chen, Y. J., and Yueh, K. C., Recovery of Valuable Metal from Photovoltaic Solar Cells through Extraction, IOP Conference Series: Materials Science and Engineering, Vol. 720, No. 1. IOP Publishing, 2020.
10.1088/1757-899X/720/1/012007Lee, J. K., Lee, J. S., and Ahn, Y. S., Photovoltaic Performance of c-Si Wafer Reclaimed from End-of-life Solar Cell using Various Mixing Ratios of HF and HNO
3, Solar Energy Materials and Solar Cells, Vol. 160, pp. 301-306, 2017.
10.1016/j.solmat.2016.10.034Kartohardjono, S., Merry, C., and Rizky, M. S., Nitrogen Oxide Reduction through Absorbent Solutions Containing Nitric Acid and Hydrogen Peroxide in Hollow Fiber Membrane Modules, Heliyon, Vol. 5, No. 12, e02987, 2019
10.1016/j.heliyon.2019.e0298731872135PMC6911882Peiliang, S., Cheng, X., and Wang, Z., NO
x Reduction by CO over ASC Catalysts in a Simulated Rotary Reactor: Effect of Reaction Conditions, Journal of the Energy Institute, Vol. 92, No. 3, pp. 488-501, 2019.
10.1016/j.joei.2018.04.009Mohan, S., Dinesha, P., and Shiva K., NO
x Reduction Behaviour in Copper Zeolite Catalysts for Ammonia SCR Systems: A Review, Chemical Engineering Journal, Vol. 384, 123253, 2020.
10.1016/j.cej.2019.123253Ministry of Environment (South Korea), Air Pollutant Emission Standards, 2014.
Noh, M. H., Lee, J. K., and Ahn, Y. S., Photovoltaic Performance of Crystalline Silicon Recovered from Solar Cell Using Various Chemical Concentrations in a Multi-Stage Process, Korean Journal of Materials Research, Vol. 29, No. 11, pp. 697-702, 2019.
10.3740/MRSK.2019.29.11.697Kamberović, Ž., Ranitović, M., and Korać, M., Hydrometallurgical Process for Selective Metals Recovery from Waste-printed Circuit Boards, Metals, Vol. 8, pp. 441, 2018.
10.3390/met8060441Fischer-Cripps, A. C., The Chemistry Companion, CRC Press, 2011.
10.1201/b11016Polani, S., Melamed, S., and Burlaka, L., Large-scale Synthesis of Polyhedral Ag Nanoparticles for Printed Electronics, RSC Advances, Vol. 7, pp. 54326-54331, 2017.
10.1039/C7RA11370FBühler, J., Steiner, F-P., and Baltes, H., Silicon Dioxide Sacrificial Layer Etching in Surface Micromachining, Journal of Micromechanics and Microengineering, Vol. 7, pp. 1-13, 1997.
10.1088/0960-1317/7/1/001Park, H. S., Cho, J. H., and Jung, J. H., A Review of Wet Chemical Etching of Glasses in Hydrofluoric Acid Based Solution for Thin Film Silicon Solar Cell Application, Current Photovoltaic Research, Vol. 5, No. 3, pp. 75-82, 2017.
Ritala, H., Kiihamäki, J., and Heikkilä, M., Studies on Aluminium Corrosion during and after HF Vapour Treatment, Microelectronic Engineering, Vol. 87, pp. 501-504, 2010.
10.1016/j.mee.2009.07.005Abd El Aal, E. E., Abd El Wanees, S., and Farouk, A., Factors Affecting the Corrosion Behaviour of Aluminium in Acid Solutions. II. Inorganic Additives as Corrosion Inhibitors for Al in HCl Solutions, Corrosion Science, Vol. 68, pp. 14-24, 2013.
10.1016/j.corsci.2012.09.038












